Can we help you?
Contact us

Can we help you?
Contact us

Thank you for contacting us
Your form has been submitted successfully Our team will contact you again as soon as possible.
Whooppss...!! An error has occurred
Try sending later or write an email directly to areaempresas@ua.es

 PATENTED TECHNOLOGY
PATENTED TECHNOLOGY
INFO
SHEET
DOWNLOAD
EXECUTIVE
ABSTRACT
CONTACT DETAILS:
Relaciones con la Empresa
Oficina de Transferencia de Resultados de la Investigación-OTRI
Universidad de Alicante
Tel.: +34 96 590 99 59
Email: areaempresas@ua.es
http://innoua.ua.es
El grupo de investigación ha desarrollado y optimizado un proceso altamente enantioselectivo catalizado por pequeñas cantidades de un complejo de plata catiónica con ligandos del tipo fosforamidito quiral, que permite generar pirrolidinas polisustituidas enantioméricamente enriquecidas, las cuales dan lugar a derivados de prolina sustituidas tras una secuencia sintética de tres pasos. Estas prolinas se utilizan como agentes antivirales de demostrada eficacia en la lucha contra el virus que causa la hepatitis C. Su administración permite reducir la cantidad de fármaco suministrado al paciente, así como mitigar los efectos secundarios de las actuales terapias. El grupo busca empresas interesadas en adquirir esta tecnología para su explotación comercial.

La terapia que se utiliza actualmente está basada en la combinación del interferón ¿ pegilado con el agente antiviral ribavirina. El 50% de los pacientes sometidos a este tratamiento han sido capaces de combatirlo eficazmente, aunque con efectos secundarios agudos como anemia, neutropenia, trombocitopenia, dolor muscular, fatiga, cefaleas, alteraciones psiquiátricas, insomnio, alopecia, anorexia, alergias, etc.
Otro inconveniente es la elevada cantidad de fármaco suministrado por kg de peso, lo que acentúa mucho más los efectos adversos. Por estas razones, el desarrollo de nuevas terapias para tratar y combatir esta infección resulta de importancia capital La polimerasa de ARN del virus es vital para su replicación. Se trata de una enzima muy bien caracterizada donde los dominios activos que deben ser
bloqueados por los inhibidores están perfectamente identificados. Uno de los mejores y más eficaces inhibidores corresponde a la familia de las pirrolidinas sustituidas.
Hasta ahora, todas las síntesis realizadas de las mencionadas estructuras pirrolidínicas se basan en reacciones de cicloadición 1,3-dipolares a temperaturas elevadas utilizando metalo-dipolos derivados de metales alcalinos y de transición. En todos los casos, los productos obtenidos son mezclas racémicas o una mezcla de diastereoisómeros, por lo que para aislar cada enantiómero por separado se recurre a la técnica de HPLC quiral semipreparativa o a la resolución del racemato empleando el ácido fosfórico derivado del 1,1¿-binaft-2,2¿-ol.
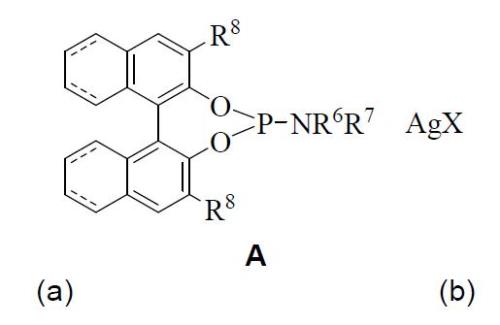
caracterizado por la coordinación de fosforamidito quiral (a) y de sal de plata catiónica (b); donde R6 es hidrógeno o un radical seleccionado del grupo que comprende un alquilo (C1-C6), un arilo (C5-C14) o un arilalquilo; R7 es hidrógeno o un radical seleccionado del grupo que comprende un alquilo (C1-C6), arilo (C5-C14) o arilalquilo; R8 es hidrógeno o un radical seleccionado del grupo que comprende alquilo (C1-C6), alcoxialquilo, (dialquilamino)alquilo (C1-C6) o arilo; X se selecciona de la lista que comprende fluoruro, acetato, perclorato, trifluorometanosulfonato, tetrafluoroborato, nitrato, hexafluorofosfato o hexafluoroantimoniato; y (---) representa un enlace que puede existir o no. También se ha desarrollado y optimizado el procedimiento para preparar el complejo metálico quiral que presenta la fórmula general B: 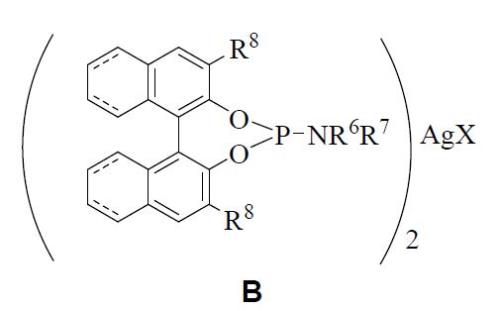
caracterizado por la coordinación de dos equivalentes del fosforamidito quiral (a) y un equivalente de sal de plata catiónica (b); donde R6 a R8 y X se han descrito anteriormente.
Estos complejos (A y B) se preparan poniendo en contacto uno o dos equivalentes, respectivamente, de fosforamidito quiral (a), con un equivalente de sal de plata catiónica (b) en presencia de un disolvente orgánico, ausencia de luz y a temperatura ambiente.
También se ha optimizado la reacción 1,3-dipolar enantioselectiva de iluros de azometino derivados de iminoésteres (V) con sistemas acrílicos (VI) catalizada por cantidades subestequiométricas de los citados complejos de plata quirales 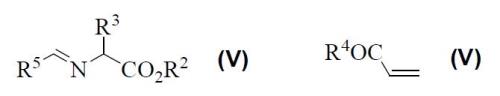
donde R2 es un alquilo (C1-C6), R3 es un alquilo (C1-C6) o arilalquilo, R4 es un radical que se selecciona de la lista que comprende alcoxi, alquilamino, arilamino o dialquilamino, y R5 es heteroarilo. Se obtiene así una serie de intermedios y productos finales que comparten las fórmulas generales (I) ó (II) siguientes: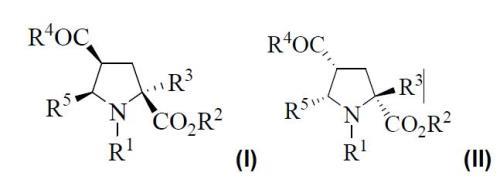
donde los radicales R1 a R5 pueden ser: R1 un hidrógeno o un aroílo, R2 un hidrógeno o un alquilo (C1-C6), R3 un alquilo (C1-C6) o arilalquilo, R4 un radical que se selecciona de la lista que comprende hidroxi, alcoxi, alquilamino, arilamino o dialquilamino, y R5 un heteroarilo.
Los compuestos antivirales derivados de prolina enriquecidos enantioméricamente, presentan una fórmula general (I) ó (II) donde R1 es aroílo, R2 es hidrógeno, R3 es alquilo (C1-C6) o arilalquilo, R4 es hidroxi, alquilamino, arilamino o dialquilamino, y R5 es heteroarilo.
El grupo aroílo de los compuestos antivirales es de crucial importancia en la actividad inhibidora del virus de la hepatitis C, ya que es la parte de la molécula que facilita la permeabilidad a través de las membranas celulares.
También se ha desarrollado un compuesto de fórmula general C: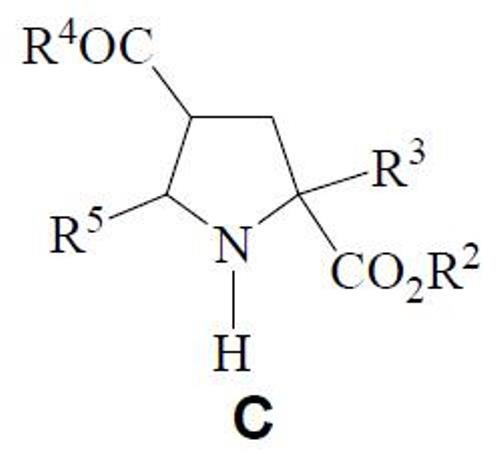
donde R2 es un alquilo (C1-C6), R3 es un alquilo (C1-C6) o arilalquilo, R4 es un radical que se selecciona de la lista que comprende alcoxi, alquilamino, arilamino o dialquilamino, y R5 es heteroarilo.
Las configuraciones absolutas de C son las siguientes: C(I)=(2S,4S,5R) y C(II)=(2R,4R,5S):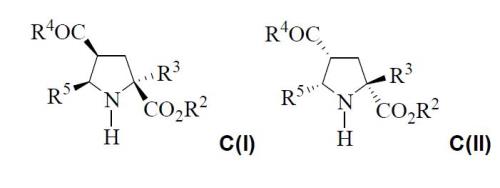
A partir de C, se ha sintetizado un compuesto de fórmula general D: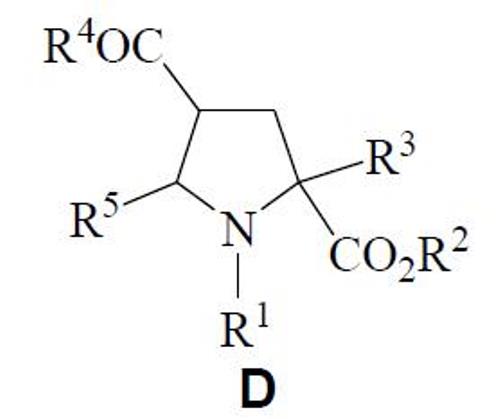
donde R1 es aroílo y de R2 a R5 como se ha descrito anteriormente.
Las configuraciones absolutas de D son las siguientes: D(I)=(2S,4S,5R) y D(II)=(2R,4R,5S): Finalmente, se ha preparado un compuesto de fórmula general E a partir de D: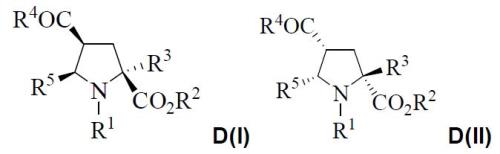
Finalmente, se ha preparado un compuesto de fórmula general E a partir de D:
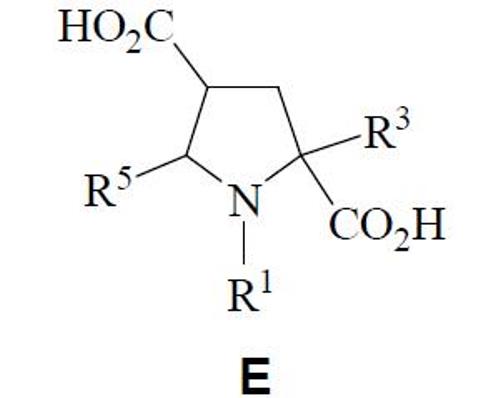
donde R1 es aroílo, y R3 y R5 como se han descrito anteriormente.
Las configuraciones absolutas de E son las siguientes: E(I)=(2S,4S,5R) y E(II)=(2R,4R,5S):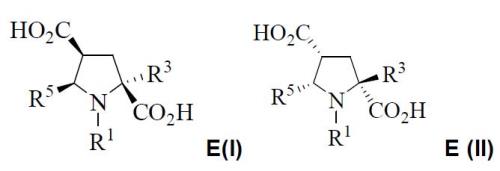
PRINCIPALES VENTAJAS:
· Se consiguen procesos altamente enantioselectivos (elevado exceso enantiomérico).
· El producto obtenido presenta una conversión muy elevada.
· Procedimiento muy efectivo.
ASPECTOS INNOVADORES
Es la única metodología capaz de obtener con muy elevados excesos enantioméricos estos compuestos. Normalmente, para aislar cada enantiómero por separado, se recurre a la técnica de HPLC quiral semi-preparativa o a la resolución del racemato empleando el ácido fosfórico derivado del 1,1·-binaft- 2,2·-ol y otras técnicas adicionales.
Tras múltiples ensayos, se ha optimizado el proceso a nivel laboratorio, obteniendo:
· Purezas superiores al 97%.
· Rendimientos superiores al 70%.
· Relaciones enantioméricas, como mínimo 94:6
Respecto a su aplicación industrial, el Departamento de Química Orgánica dispone de una planta piloto totalmente equipada para su escalado a nivel preindustrial e industrial (desde el rango de los miligramos hasta lotes multikilo).
Las instalaciones cubren todo el proceso de desarrollo (producción con reactores de hasta 300 litros de capacidad, secado, tratamiento físico, almacenaje, control de proceso y análisis). Están certificadas bajo la norma ISO 9001, respetan las cGMPs (current Good Manufacturing Procedures) y trabajan en condiciones de perfecta trazabilidad
FARMACÉUTICO: representa un terapia muy esperanzadora en la lucha contra el virus que causa la hepatitis C. Su eficacia se ha comprobado en ratones: IC50= 0.3-0.5 ·M, (e incluso menores si se tienen en cuenta los últimos resultados publicados).
El grupo de investigación busca empresas interesadas en adquirir la tecnología para su explotación comercial. Para ello, está dispuesto a firmar cualquiera de las diferentes formas de transferencia de tecnología (licencia de la patente, cesión, etc.).
La tecnología se encuentra protegida bajo patente:
· Número de patente internacional: WO2009/121989 A1
· Fecha de publicación internacional: 08.10.2009
Medicina y Salud
Tecnología Química
Carretera San Vicente del Raspeig s/n - 03690 San Vicente del Raspeig - Alicante
Tel.: (+34) 965 90 9959




